Zum ersten mal haben Wissenschaftler nutzten die CRISPR-gen-editing-tool, um erfolgreich zu behandeln, eine genetische Muskel-Erkrankung in einem lebenden Erwachsenen Säugetieren. Es ist eine vielversprechende medizinische Durchbruch, könnte schnell dazu führen, menschliche Therapien.
Wissenschaftler haben gekämpft, zur Behandlung von Duchenne-Muskeldystrophie seit Jahrzehnten. Bisher haben Ihre Bemühungen konzentrierten sich auf die Behandlung von kultivierten Zellen in Petrischalen, oder bei dem Versuch, um CRISPR/cas9, eine mächtige DNA cut-and-paste-tool, um die reparierten Kopie des Defekten Gene effektiv und sicher. Jetzt, mit Hilfe eines speziell modifizierten virus, Forscher von der Duke University haben bestätigt, eine vielversprechende Lösung mit live-Maus-Modelle. Das team der Studie erscheint in der aktuellen Ausgabe von Science.
Duchenne-Muskeldystrophie ist eine Muskel-verschwenden Krankheit, die sich auf einem 5.000 Neugeborenen Männchen. Die genetische Fehler ist auf dem X-Chromosom, so dass Mädchen mit zwei X-Chromosomen haben tendenziell mindestens eine funktionierende Kopie des Gens. Symptome erscheinen in der Regel zwischen 3 und 5, nach dem die Krankheit schreitet schnell. Die meisten Jungen sind nicht in der Lage, zu Fuß durch die Zeit, die Sie jetzt 12, und Sie brauchen schließlich eine Atemschutzmaske zu atmen. Die Lebenserwartung liegt zwischen 20 bis 30 Jahren.
Die genetische Störung, die durch das fehlen von dystrophin, eine kritisch wichtige langen protein-Kette, die die Unversehrtheit der Muskeln. Dystrophin, kodiert durch ein gen mit fast 80 protein-kodierende Regionen genannt exons. Selbst wenn nur ein einziges exon stark mutiert, die Kette wird nicht gebaut werden. Und ohne dystrophin, Muskeln langsam verschlechtern.
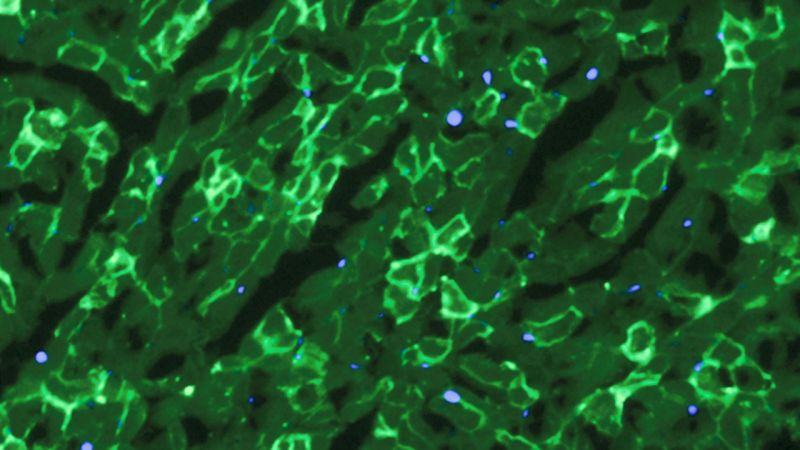
Die restaurierten der Produktion von dystrophin (light green) in den Muskelzellen von Mäusen. Credit: C. E. Nelson et al., 2015
Der Herzog Forscher, geführt von der Genetiker Chris Nelson, verwendet CRISPR/cas9 zu entfernen, die problematisch DNA verhindert, dass die Zellen aus der Produktion von dystrophin.
Gesponsert
CRISPR, ein tool, dass sich nur drei Jahren, die es Wissenschaftlern ermöglicht, Bearbeiten Genome mit einer unglaublichen Präzision und Flexibilität. Wie eine person, die versucht zu lösen eines Puzzles, das system verwendet synthetische DNA bekannt als CRISPRs Scannen eines Genoms auf der Suche nach der richtigen Stelle. Ein protein namens cas9 wirkt wie eine Schere, Schnitt durch die DNA.
Liefern diese genetischen Veränderungen, die Herzog Forscher verwendeten eine Art von nicht-pathogenen virus. “Eine große Hürde für die gen-Bearbeitung Lieferung. Wir wissen, was Gene, die behoben werden müssen, die für bestimmte Krankheiten, sondern immer den gen-editing-tools, wo Sie gehen müssen, ist eine riesige Herausforderung”, sagte Nelson in einer Pressemitteilung. “Der beste Weg, wir müssen es jetzt tun, ist das ausnutzen von Viren, weil Sie haben Milliarden von Jahren weiterentwickelt, um herauszufinden, wie Sie Ihre eigenen viralen Gene in die Zellen.”
Für die Studie, die Forscher arbeiteten mit genetisch veränderte Mäuse, die lähmenden mutation auf einem der exons des dystrophin-Gens. Die Wissenschaftler programmiert die neue CRISPR/cas9-Systems, Unkraut aus den dysfunktionalen exon, verlassen der Körper die Natürliche repair-system zu Nähen die übrigen gen wieder zusammen. Das Ergebnis war eine verkürzte, aber funktional, version des Gens.
Um die zu erreichen jeder Muskel war das virus in die Blutbahn gespritzt werden von den Mäusen. Ergebnisse zeigten messbare Korrekturen von Muskeln im ganzen Körper, einschließlich der Herz—ein besonders wichtiges Ergebnis, wenn man bedenkt, dass die Herzinsuffizienz ist die häufigste Todesursache bei Duchenne-Patienten.
Aber die Mäuse erhalten, dass die Therapie nicht so gut wie normale Mäuse auf Muskel-tests, so dass es nicht zu einer Heilung. Das heißt, die Forscher glauben, es gibt viel Raum für Verbesserungen, und, dass über 80 Prozent der Menschen mit DMD könnten davon profitieren, dass eine fehlerhafte exon entfernt.
“Es ist immer noch eine erhebliche Menge an Arbeit zu tun, um zu übersetzen, um eine menschliche Therapie und zeigen Sicherheit”, sagte Herzog Forscher Charles A. Gersbach. “Aber diese Ergebnisse kommen von unserer ersten Experimente sind sehr spannend. Von hier aus werden wir die Optimierung der Transport-system, das die Bewertung der Ansatz in schwereren Modelle von DMD, und die Beurteilung der Leistungsfähigkeit und Sicherheit in größere Tiere mit dem letztendlichen Ziel, sich in klinischen Studien.”
Zwei weitere teams, die alle unabhängig voneinander erzielt ähnliche Ergebnisse Ihrer Forschung. Diese Studien wurden von Eric Olson an der University of Texas Southwestern Medical Center und Amy Wette an der Harvard University.
Im Gegensatz zu den Bemühungen zum ändern der Keimbahn des embryos, diesen besonderen Ansatz angewendet werden können, um ein lebendiges Wesen. Dies bedeutet, dass die genetische änderungen können später im Leben, und Sie sind nicht vererbbar.
“Die jüngsten Diskussion über die Verwendung von CRISPR zu korrigieren genetische Mutationen in menschlichen Embryonen zu Recht hat generiert erhebliche Bedenken in Bezug auf die ethischen Implikationen eines solchen Ansatzes,” sagte Gersbach “Aber CRISPR zu korrigieren genetische Mutationen in den betroffenen Geweben von Kranken ist nicht umstritten. Diese Studien zeigen, dass ein Pfad, wo das möglich ist, aber es gibt noch eine Menge Arbeit zu tun.”
[Duke University, New York Times, Wissenschaft AAAS]
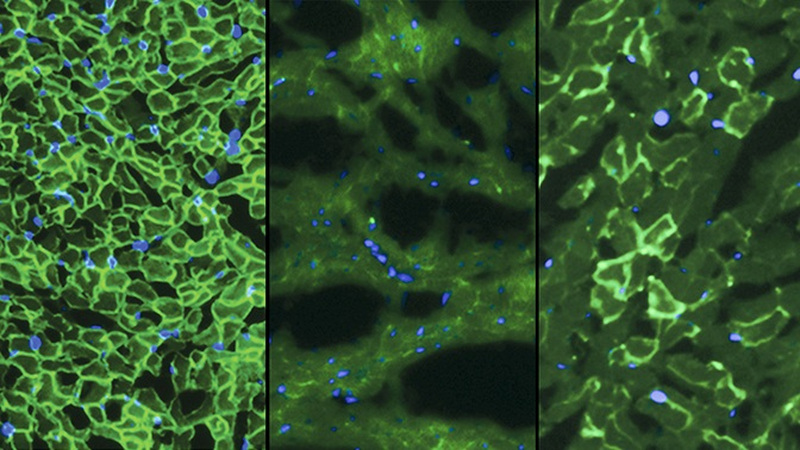
Den Autor E-Mail an george@gizmodo.com und ihm Folgen unter @dvorsky. Bild oben: Dystrophin (hellgrün) zu sehen ist im Herzmuskel von normalen Mäusen (Links), fehlt bei Mäusen mit DMD (Mitte) und teilweise restauriert, in Duchenne-Mäuse behandelt mit CRISPR/Cas9 (rechts). Credit: C. E. Nelson et al., 2015