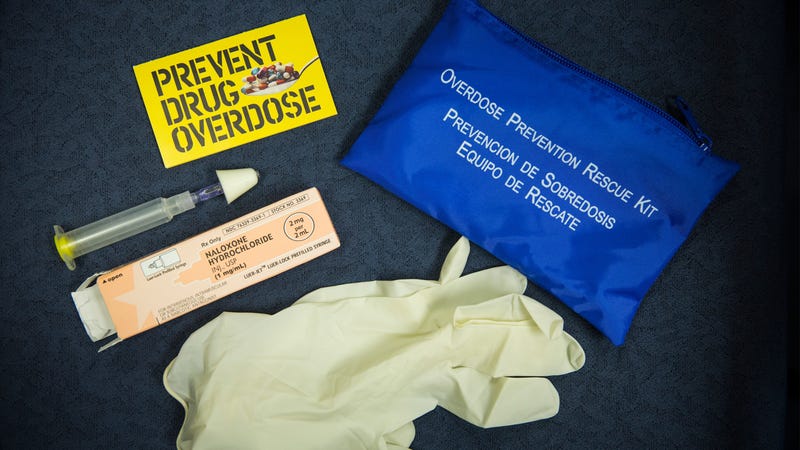
 Bild: Andrew Burton (Getty Images)
Bild: Andrew Burton (Getty Images)
Einer der wichtigsten Anstifter für die opioid-Krise ist auf der Suche, um zu verkaufen, eigene Droge, um Menschen zu retten, von tödlichen überdosierungen—aber die Gesellschaft tut es nicht einstecken, die Gewinne.
Diese Woche, die Droge Unternehmen Purdue Pharma hat angekündigt, dass seine experimentelle opioid-überdosierung Antidot wurde erteilt “Fast Track” Bezeichnung von der Food and Drug Administration. Der status gemeint ist, zu beschleunigen der Prozess der überprüfung von neuen Medikamenten für schwere Bedingungen, die nicht anderweitig abgedeckt durch vorhandene Behandlungen. In diesem Fall, Purdue behauptet, dass seine Droge, abgeleitet aus der opioid-antagonist nalmefene, könnte eine stärkere, länger anhaltende version von Naloxon, das einzige derzeit zugelassene Medikament zur Umkehrung der Effekte, die eine opioid-überdosierung im Notfall.
Purdue aggressive Vermarktung Ihrer wertvollen opioid-Schmerzmittel Oxycodon bereits eine entscheidende Rolle gespielt in der Fahrt bis raten von opioid-Einsatz Störung unter den Amerikanern in den 1990er und 2000er Jahren. Und auch, nachdem das Unternehmen und seine Führungskräfte bekannten sich schuldig, um Irreführung der öffentlichkeit über die Droge, die Risiken in 2007 -, state-und county Klagen beschuldigt haben Purdue weiterhin zu profitieren trügerisch opioid-marketing, alle, während Sie auf einem Auge blind auf ärzte, die überschwemmt den Schwarzmarkt mit Ihren Drogen oder anderen gefährlichen Dosen an Patienten.
Es ist aus einer dieser Klagen, eingereicht von der Massachusetts Attorney General, dass wir wissen, dass dies nicht das erste mal, Purdue hat, schwebte die Idee, den Verkauf einer überdosis Behandlung neben den Schmerzmitteln.
Nach dokumentarischen Beweise gesammelt, von der Staatsanwaltschaft und da sind das Gericht, der Purdue Führungskräfte Sprachen über Ihre Hoffnungen der Eintritt in den lukrativen und “attraktive” Markt der sucht Behandlung so früh wie 2014—sogar so weit gehen zu kommen mit einem code-Namen Project Tango. Zu der Zeit wog Sie den Kauf der Rechte zu verkaufen, Narcan, der Markenname-spray version von Naloxon, und Suboxone verkauft, eine version des opioid-craving und entzugssymptome Droge Buprenorphin verabreicht durch einen film, der unter die Zunge gelegt. In einer Erklärung zu Propublica-und Stat-News im Januar dieses Jahres Purdue sagte, es hatte schließlich beschlossen, gegen bewegen. Stattdessen scheint es, es hat sich auf Wettbewerb mit Narcan statt.
In der Hoffnung zur Eindämmung einige der vorhergesagten Spielraum, obwohl der finanziell angeschlagenen Unternehmen versprach in seiner Ankündigung, es würde “die Arbeit voran zu bringen diese option mit der Verpflichtung nicht auf profit aus jedem zukünftigen Verkauf dieser Droge.” Im letzten Herbst, ist er auch verpflichtet, zu Spenden $3,4 Millionen an die non-profit-Harm Reduction-Therapeutika zu helfen, Fonds für Entwicklung der generischen version eines Naloxon-spray.
Purdue experimentelles Medikament würde nicht unbedingt viel von einer cash-cow. Seine version von nalmefene, eine Injektion von nalmefene-Hydrochlorid (HCI), wurde bereits von der FDA zugelassen als eine Umkehrung der opioid-Medikament im Jahr 1995, unter dem Namen Revex. Aber von 2009, das Medikament die Hersteller entscheidet, die Produktion einzustellen Revex, behauptete, es war einzig und allein aus geschäftlichen Gründen. Eine spätere Untersuchung durch die FDA, freigegeben im Jahr 2017 wird festgestellt, dass Revex war nicht ad Acta gelegt, weil es nicht funktioniert hat oder hatte gefährliche Nebenwirkungen. (In der Tat, nalmefene ist derzeit zugelassen zur Behandlung von Alkoholabhängigkeit in der EU).
Die Entscheidung, die Agentur Hinzugefügt, auch wurde der Weg für die Zulassung von nalmefene HCI in Zukunft wieder mit wenig Aufwand. Und mindestens einen anderen pharmazeutischen Unternehmen, mit dem Segen der Bundesregierung, verfolgt eine eigene Nasenspray-version von nalmefene.
Teilen Sie Diese Geschichte