For første gang nogensinde, at forskere har brugt den CRISPR gen-redigering værktøj til succes behandle en genetisk muskellidelse i et levende voksent pattedyr. Det er en lovende medicinske gennembrud, der snart kunne føre til menneskelige behandlinger.
Forskere har kæmpet til behandling af Duchennes muskeldystrofi i årtier. Til dato, og deres indsats har været fokuseret på behandling af dyrkede celler i petriskåle, eller i at forsøge at få CRISPR/cas9, en stærk DNA-cut-and-paste af, at levere den repareret kopi af det defekte gener, effektivt og sikkert. Nu, ved hjælp af et specielt modificeret virus, forskere fra Duke University har bekræftet en lovende løsning er at bruge live mus modeller. Holdet ‘ s undersøgelse, der vises i den seneste udgave af Science.
Duchennes muskeldystrofi er en muskel, der spilder sygdom, der påvirker én ud på 5.000 nyfødte hanner. Den genetiske fejl er på X-kromosomet, så piger med to X-kromosomer, har tendens til at have mindst en fungerende kopi af genet. Symptomer, der typisk optræder i alderen 3 og 5, efter hvilken lidelse udvikler sig hurtigt. De fleste drenge er ude af stand til at gå ved den tid, de er 12, og de i sidste ende har brug for en respirator til at trække vejret. Den forventede levetid er mellem 20 og 30 år.
Den genetiske lidelse er forårsaget af mangel på dystrofin, en kritisk vigtige lang protein kæde, der opretholder integriteten af muskler. Dystrofin er kodet af et gen, som indeholder næsten 80 protein-kodende regioner kaldes exons. Hvis selv en enkelt exon er dårligt muteret, kæden ikke bliver bygget. Og uden dystrofin, muskler langsomt forværres.
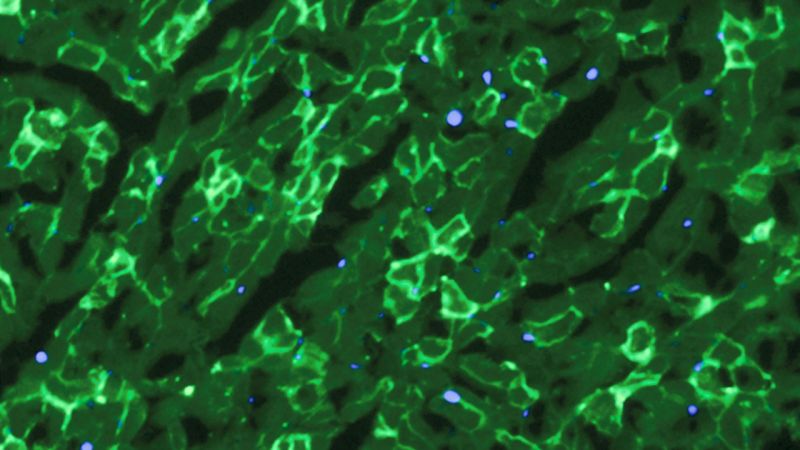
Den restaurerede produktionen af dystrofin (lys grøn) i muskelcellerne af mus. Kredit: C. E. Nelson et al., 2015
Hertugen forskere, ledet af genetiker Chris Nelson, der anvendes CRISPR/cas9 at fjerne de problematiske DNA, der blev forhindrer cellerne i at producere dystrofin.
Sponsoreret
CRISPR, et værktøj, som opstod for blot tre år siden, giver forskerne mulighed for at redigere genomer med utrolig præcision og fleksibilitet. Som en person, der forsøger at løse et puslespil, systemet bruger syntetiske DNA kendt som CRISPRs at scanne et genom i jagten på det rigtige sted. Et protein kaldet cas9 fungerer som en saks til at skære gennem DNA.
At levere disse genetiske ændringer, Hertugen forskere, der anvendes en type af ikke-patogene virus. “En stor forhindring for gen redigering levering. Vi ved, hvilke gener, der skal fastsættes for visse sygdomme, men at få det gen, redigeringsværktøjer, hvor de er nødt til at gå, er en kæmpe udfordring,” sagde Nelson i en udgivelse. “Den bedste måde, vi er nødt til at gøre det lige nu, er at drage fordel af virus, fordi de har brugt milliarder af år udvikler sig til at finde ud af, hvordan de får deres egen virale gener i cellerne.”
For undersøgelsen, har forskerne arbejdet med genetisk modificerede mus, der havde den invaliderende mutation på en af de exons af dystrofin-genet. Forskerne har programmeret nye CRISPR/cas9 system til at luge ud i de dysfunktionelle exon, der forlader kroppens naturlige reparations system til at sy de resterende gen sammen igen. Resultatet blev en forkortet, men funktionelle, version af genet.
For at nå hver eneste muskel, og virus blev sprøjtet ind i blodbanen af mus. Resultaterne viste målbare korrektioner af muskler i hele kroppen, herunder hjerte—et særligt vigtigt resultat, i betragtning af, at hjertesvigt er en væsentlig årsag til dødsfald blandt Duchenne-patienter.
Men de mus, der fik terapi ikke gøre det så godt som normale mus på muskel test, så det er ikke en kur. Når det er sagt, forskere mener, at der er masser af plads til forbedring, og at op mod 80 procent af personer med DMD kunne drage fordel af at have en defekt exon fjernet.
“Der er stadig et betydeligt arbejde at gøre for at oversætte dette til en human behandling og demonstrere sikkerhed,” sagde Hertugen forsker Charles A. Gersbach. “Men disse resultater, der kommer fra vores første forsøg er meget spændende. Fra her, vil vi være på at optimere leveringen system, evaluering af den tilgang, der i mere alvorlige modeller af DMD, og vurdering af effektivitet og sikkerhed i de større dyr med det endelige mål for at komme ind i kliniske forsøg.”
To andre hold—alle, der arbejder uafhængigt af hinanden—har opnået lignende resultater i deres forskning. Disse undersøgelser blev udført af Eric Olson på University of Texas Southwestern Medical Center og Amy Satse på Harvard University.
I modsætning til bestræbelser på at ændre den germline af embryoner, denne særlige fremgangsmåde kan anvendes til et levende væsen. Dette betyder, at de genetiske ændringer kan indføres senere i livet, og de er ikke arvelige.
“Den seneste debat om brug af CRISPR til at korrigere genetiske mutationer i den menneskelige embryoner har med rette vakt betydelig bekymring med hensyn til de etiske konsekvenser af en sådan tilgang,” sagde Gersbach “, Men ved hjælp af CRISPR til at korrigere genetiske mutationer i de berørte væv af syge patienter, der ikke er under forhandling. Disse undersøgelser viser en vej, hvor det er muligt, men der er stadig en betydelig mængde af arbejde at gøre.”
[Duke University, New York Times, Videnskab AAAS]
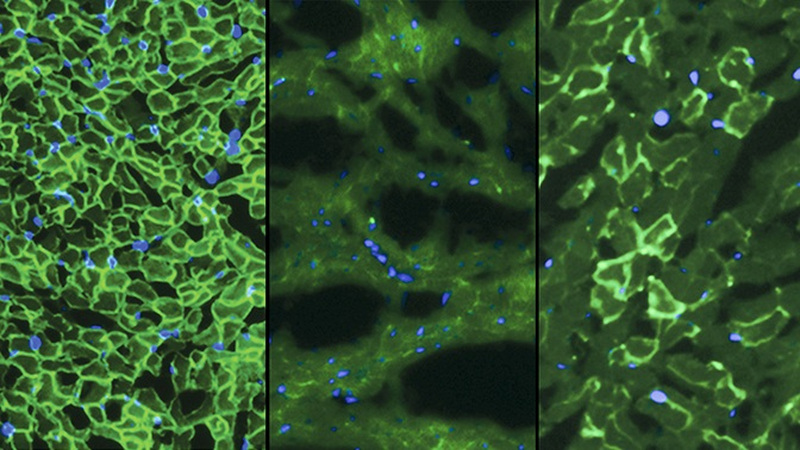
E-mail forfatteren på george@gizmodo.com og følge ham på @dvorsky. Øverste billede: Dystrophin (lys grøn) er set i hjertemusklen fra normale mus (til venstre), mangler i mus med DMD (i midten), og delvist restaureret i Duchenne mus behandlet med CRISPR/Cas9 (til højre). Kredit: C. E. Nelson et al., 2015